双原子
$^{2S+1}\Lambda$简单确定方法
根据分子轨道占据来确定双原子的分子光谱项为$^{2S+1}\Lambda$:
- 首先根据确定$2S+1$
- $\Lambda$的确定根据单电子所占据的轨道对应的序号进行加合,注意除了σ以外,其他分子轨道都有简并轨道,因此一个是$\lambda$,一个是$-\lambda$,比如eg.1和eg.2的区别
| $\lambda$ | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|---|---|
| 分子轨道符号 | $\sigma$ | $\pi$ | $\delta$ | $\phi$ | $\gamma$ | $\eta$ | $\iota$ |
| $\Lambda$ | $\Sigma$ | $\Pi$ | $\Delta$ | $\Phi$ | $\Gamma$ | $H$ | $I$ |
当电子态为$\Sigma$时:
- 波函数关于键轴的平面$σ_{xz}$为对称需要用$+$表示,反对称用$-$表示。
- 简单判断方法是简并轨道中有一个轨道是关于σxz对称(假设为+$\lambda$),一个是关于σyz(即关于σxz反对称,假设为-$\lambda$)。规定占据并且+$\lambda$↑为+,改变一个因素乘负号,则+$\lambda$↓、-$\lambda$↑为-,-$\lambda$↓为正,然后多个$\lambda$相乘,最后得到正负号。
- 对于同核双原子分子,如果关于对称中心$i$对称用$g$,反对称用$u$表示。
例子:$\phi^1\delta^1\pi^1$(用——依次分别代表+$\lambda$和-$\lambda$)
| eg. | $\phi^1$ | $\delta^1$ | $\pi^1$ | $\Lambda$ | $σ_{xz}$ | 分子光谱项 |
|---|---|---|---|---|---|---|
| 1 | ↑— | ↑— | ↑— | $3+2+1=6=I$ | $^4I$ | |
| 2 | ↑— | ↑— | —↑ | $3+2-1=5=H$ | $^4H$ | |
| 3 | ↑— | —↑ | —↑ | $3-2-1=0=\Sigma$ | $^4\Sigma^+$ | |
| 4 | —↑ | ↑— | ↑— | $-3+2+1=0=\Sigma$ | $^4\Sigma^-$ | |
| 5 | ↑— | —↑ | ↓— | $3-2+1=2=\Delta$ | $^2\Delta$ | |
| 6 | —↑ | ↑— | ↓— | $-3+2+1=0=\Sigma$ | $^2\Sigma^+$ | |
| 7 | —↑ | ↓— | ↓— | $-3+2+1=0=\Sigma$ | $^2\Sigma^-$ |
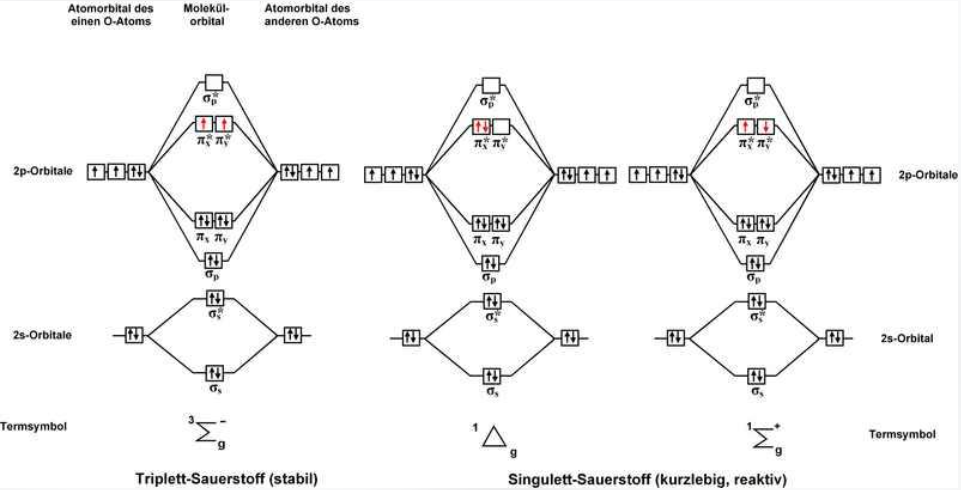
例子:O2
- $^3\Sigma^-_g$:$1-1=0=\Sigma$,$+*-=-$
- $^1\Sigma^+_g$:$1-1=0=\Sigma$,$+*+=+$
摘选自DeepSeek
对重元素(如镧系、锕系),SOC 效应显著,自旋角动量和轨道角动量发生耦合,此时需引入 总角动量投影 $\Omega$,定义为:,($\Sigma$是自旋角动量在分子轴上的投影)。
- 例如:假设某个态的 Λ=2(Δ 态),自旋 S=1(三重态),则可能的 Σ = -1, 0, +1,对应的 Ω = |2−1|=1、|2+0|=2、|2+1|=3,最终分裂成 Ω=1, 2, 3 三个态。
$^{2S+1}\Lambda_\Omega$中$\Omega$的确定
$\Omega$为$\pm{(S+\Lambda)}$,$\pm{(S+\Lambda-1)}$……一共$2(S+\Lambda)+1$项
例子:$^4H$中$S+\Lambda=\frac{3}{2}+5=\frac{13}{2}$,则$\Omega$为$\pm\frac{13}{2}$,$\pm\frac{11}{2}$,$\pm\frac{9}{2}$,$\pm\frac{7}{2}$,$\pm\frac{5}{2}$,$\pm\frac{3}{2}$,$\pm\frac{1}{2}$一共14项。
单原子
等价电子原子光谱
- 首先根据确定$2S+1$(即单电子数+1)
- 轨道角动量量子数L等于每个电子的轨道角量子数矢量和(电子从最高的轨道角量子数的轨道开始占据),根据和确定符号,再确定J=L-S
| L(l之和) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 符号 | S | P | D | F | G | H | I | K | L | M | N | O |
例子:
| U(II) | U(III) | U(IV) | U(V) | U(VI) | |
|---|---|---|---|---|---|
| L | 3+2+1+0=6 | 3+2+1=6 | 3+2=5 | 3 | 0 |
| L-S | 6-2=4 | 6-3/2=9/2 | 5-1=4 | 3-1/2=5/2 | 0-0=0 |
